Содержание
- 2. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ - явления, связанные с существованием межфазных границ. В области контакта двух фаз происходит образование
- 3. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ Толщина поверхностного слоя определяется радиусом действия поверхностных сил .
- 4. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ Поверхностные слои неоднородны в масштабе молекулярных размеров, отличаются от объёмных фаз физическими свойствами, молекулярным
- 5. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ В поверхностных слоях наблюдаются специфические химические эффекты, вплоть до изменения валентности.
- 6. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ Особыми свойствами обладают и родственные поверхностным слоям малые объекты - ТОНКИЕ ПЛЁНКИ И НИТИ,
- 7. Поверхностные явления Внутри жидкости силы уравновешиваются Со стороны газа равнодействующая, направлена внутрь жидкости и поверхность раздела
- 8. Поверхностные явления Увеличение площади поверхности раздела фаз связано с переходом молекул из глубины фазы на поверхность,
- 9. Поверхностное натяжение σ — это работа, необходимая для создания 1 м2 поверхности [σ]= Дж/м2 Поверхностное натяжение
- 10. Поверхностное натяжение Поверхностное натяжение зависит от: природы жидкости σ(Н2О)=72,8 Дж/м2; σ(сыворотки крови)=45,4 Дж/м2). температуры. давления. концентрации
- 11. Методы определения поверхностного натяжения Методы определения поверхностного натяжения делятся на статические и динамические. В статических методах
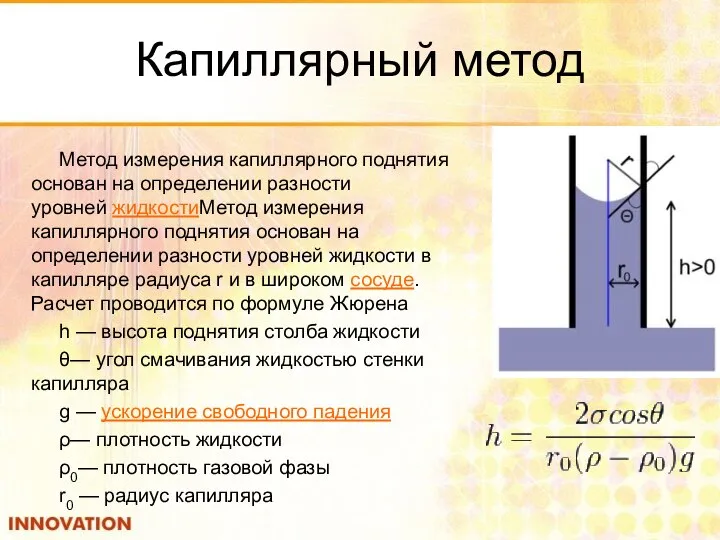
- 12. Капиллярный метод Метод измерения капиллярного поднятия основан на определении разности уровней жидкостиМетод измерения капиллярного поднятия основан
- 13. Методы определения поверхностного натяжения Динамические методы связаны с разрушением поверхностного слоя. Динамические методы могут быть применены
- 14. Метод бегущих волн При возмущении жидкости пластиной «лежащей» на её поверхности, по ней начинает распространяться круг
- 15. Когезия Взаимодействие (сцепление) молекул, атомов, ионов внутри одной фазы называют КОГЕЗИЕЙ.
- 16. Когезия. Работа когезии Работа когезии определяется затратой энергии па обратимый изотермический разрыв тела по сечению, равному
- 17. Когезия Когезия отражает межмолекулярное взаимодействие внутри гомогенной фазы, поэтому ее могут характеризовать также такие параметры, как
- 18. Когезия В уравнение Ван-дер-Ваальса для реальных газов (р+а/V2)(V-b)=RT где р— внешнее давление; V — мольный объем
- 19. Когезия Так как мольный объем жидкостей при нормальных условиях в тысячи раз меньше мольного объема газов,
- 20. Адгезия Межфазное взаимодействие, или взаимодействие между приведенными в контакт поверхностями конденсированных тел разной природы, называют адгезией
- 21. Работа адгезии Адгезия является самопроизвольным процессом. Работа адгезии Wa, характеризующая прочность адгезионной связи, определяется работой обратимого
- 22. Работа адгезии Чтобы получить соотношение между работой адгезии и поверхностными натяжениями взаимодействующих компонентов, представим себе две
- 23. Работа адгезии Для начального и конечною состояний системы имеем Gнач=σ2,3+σ3,.1 и Gкон=σ2,3 где σ2,1, σ 3,1,
- 24. Смачивание Мерой С. обычно служит краевой угол (или угол С.) в между смачиваемой поверхностью и поверхностью
- 25. СОРБЦИЯ
- 26. Медико-биологическое значение темы: 1. Усвоение питательных и лекарственных веществ 2. Перенос О2 и СО2 из лёгких
- 27. Примеры сорбция жидкостей на твердой поверхности; сорбция газов на твердыми или жидкими поверхностями; поверхностные химические реакции:
- 28. Сорбция-изменение концентрации одного или нескольких компонентов в гетерогенной системе Сорбция – процесс поглощения одного вещества другим
- 29. Процессы, протекающие в объеме твердого сорбента Данные процессы можно разделить на: Абсорбцию; Хемосорбцию; Капиллярную конденсацию.
- 30. Адсорбция Адсорбция – самопроизвольное изменение концентрации компонента в поверхностном слое по сравнению с объемом фазы
- 31. Основные понятия Вещество, на поверхности которого происходит адсорбция, называют адсорбентом. Вещество, молекулы которого поглощаются адсорбентом, называют
- 32. Физическая адсорбция Физическая адсорбция обусловлена молекулярными или ван-дер-ваальсовыми силами.
- 33. Химическая адсорбция Химическая адсорбция или хемосорбция обусловлена химическими силами. При такой адсорбции адсорбат образует на поверхности
- 34. Количественно адсорбция может выражаться через различные величины: 1) Через предложенную Гиббсом величину Г, равную разности между
- 35. Абсолютная адсорбция Значение А не совпадает с величиной адсорбции Г т.к. оно равно общему количеству адсорбтива
- 36. Уравнение Гиббса >0 Г С вещества в поверхностном слое 0, т.е. ↑с ↓σ (ПАВ) С вещества
- 37. Уравнение Гиббса для разбавленных растворов и идеальных газов Г - количество адсорбированного вещества [моль/м2] с –
- 38. Уравнение изотермы адсорбции Полученное Гиббсом уравнение изотермы адсорбции справедливо для любых составов и различных границ раздела
- 39. Поверхностная активность Способность растворенного вещества изменять поверхностное натяжение – поверхностная активность (g) Мера поверхностной активности:
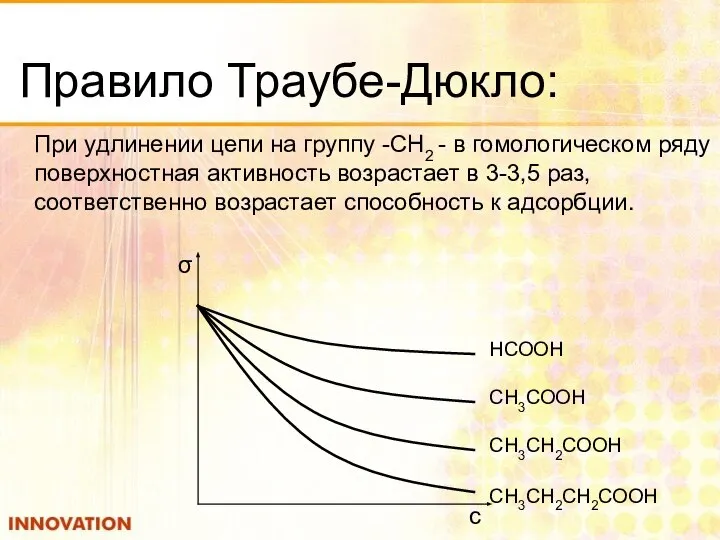
- 40. Правило Траубе-Дюкло: При удлинении цепи на группу -СН2 - в гомологическом ряду поверхностная активность возрастает в
- 41. ПАВ, ПИВ, ПНВ Поверхностно-активные вещества (ПАВ): уменьшают σ растворителя. σ раствора О. ПАВ: спирты, органические кислоты,
- 42. Изотерма поверхностного натяжения Зависимость σ от концентрации растворенного вещества при постоянной температуре – изотерма поверхностного натяжения.
- 43. Поверхностно-активные вещества (ПАВ): уменьшают σ растворителя таким образом снижается свободная энергия поверхностного слоя. Молекулы ПАВ накапливаются
- 44. Строение молекулы ПАВ: Молекула ПАВ состоит из: неполярной гидрофобной углеводородной группы (“хвост”) полярной гидрофильной группы (“голова”):
- 45. АДСОРБЦИЯ НА ГРАНИЦЕ РАСТВОР-ГАЗ
- 46. Расчет изотермы адсорбции Г= ƒ(с) Для расчета изотермы адсорбции необходимо построить зависимость σ от с. В
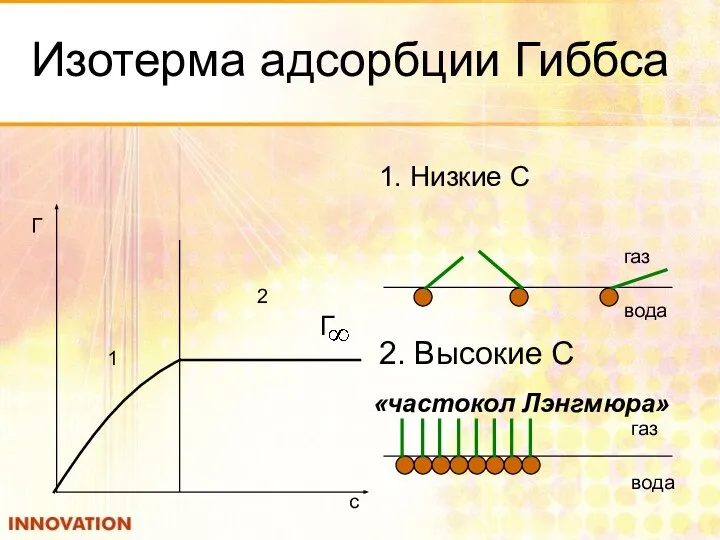
- 47. Изотерма адсорбции Гиббса 1. Низкие С 1 2 Г c газ вода 2. Высокие С газ
- 48. Уравнение Шишковского Для построения изотермы поверхностного натяжения можно воспользоваться уравнением Шишковского (используют для расчета σ жирных
- 49. Переход от уравнения Гиббса к уравнению Ленгмюра Продифференцировав уравнение Шишковского по концентрации dσ/dc=ab/(1+bc) и подставив производную
- 50. АДСОРБЦИЯ НА ГРАНИЦЕ ТВЕРДОЕ ТЕЛО-ГАЗ
- 51. Адсорбция твердыми телами Величина адсорбции зависит от: Размера поверхности адсорбента чем > Sповерхности, тем > адсорбция.
- 52. Теории адсорбции Основной задачей теории адсорбции является моделирование и математическое описание процесса адсорбции – установление зависимости
- 53. Уравнение Фрейндлиха А = x/m = k · p1/n х – количество вещества адсорбтива (моль) m
- 54. Уравнение Фрейндлиха для адсорбции из раствора на твердом адсорбенте Г = x/m = КФ · Cn
- 55. Константы адсорбции Показатель с участием константы 1/n (n) является правильной дробью и лежит в пределах: 0,2-1
- 56. Определение констант в уравнении Фрейндлиха lg A = lg k + 1/n lg c lgx/m lgA
- 57. Теория Ленгмюра Зависимость адсорбции газа на твёрдой поверхности от давления газа впервые была обоснована Ленгмюром. При
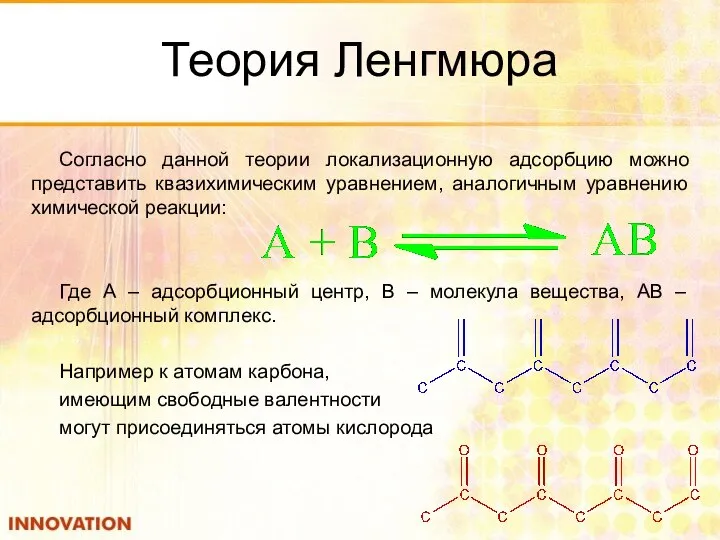
- 58. Теория Ленгмюра Согласно данной теории локализационную адсорбцию можно представить квазихимическим уравнением, аналогичным уравнению химической реакции: Где
- 59. Теория Ленгмюра Предположим, что на поверхности 1м2 часть Θ занята адсорбированными молекулами, 1-Θ свободна Скорость адсорбции
- 60. Теория Ленгмюра Скорость процесса десорбции определится по уравнению: ω2 = k2Θ, k2 – константа скорости десорбции;
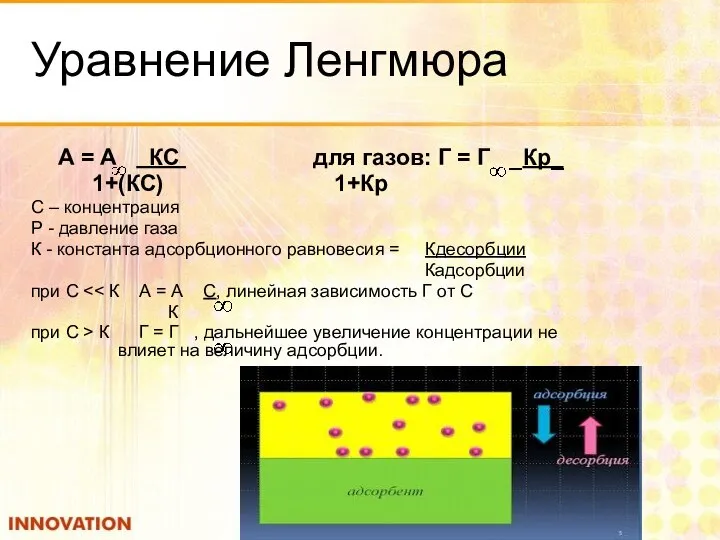
- 61. Уравнение Ленгмюра А = А КС для газов: Г = Г _Кр_ 1+(КС) 1+Кр С –
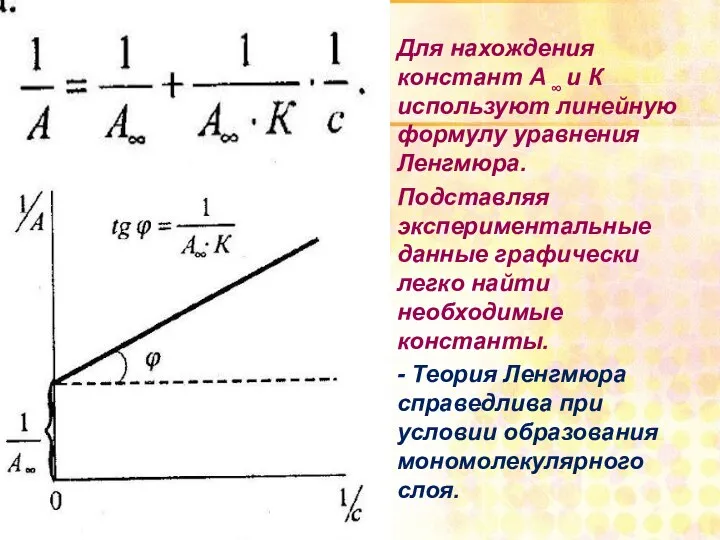
- 62. Для нахождения констант А ∞ и К используют линейную формулу уравнения Ленгмюра. Подставляя экспериментальные данные графически
- 63. Изотерма адсорбции Ленгмюра с Г
- 64. Определение площади молекулы и толщины слоя При с→∞ lim Г = Г∞ (определяют экспериментально) S =
- 65. Применение теории Ленгмюра Несмотря на то, что рассчитанные по формуле Ленгмюра данные не всегда совпадают со
- 66. Теория полимолекулярной адсорбции БЭТ (Брунауер, Эммет, Теллер) Многие экспериментальные данные свидетельствуют о том, что после образования
- 67. Теория БЭТ Изотерма І характерна для случая мономо-лекулярной адсорбции. Изотермы ІІ-V связаны с образованием нескольких слоев.
- 68. Потенциальные теории адсорбции А. Эйкен и М. Поляни (1914-1916) Авторы исключали наличие адсорбционных центров, Молекулы адсорбтива
- 69. Потенциальные теории адсорбции Данное адсорбционное поле характеризует адсорбционный потенциал ε: р0 – давление насыщенного пара над
- 70. Капиллярная конденсация Адсорбция паров пористыми телами может сопровождаться конденсацией адсорбтива в тонких порах при давлениях меньших,
- 71. Капиллярная конденсация Изотерма адсорбции, осложненная капилярной конденсацией принадлежит к одному из типов II-V по классификации Брунауэра.
- 72. Капиллярная конденсация Изотермы капиллярной конденсации А=ƒ(p/p0) используют для исследования пористой структуры сорбентов и катализаторов (V-объем жидкости,
- 73. АДСОРБЦИЯ НА ГРАНИЦЕ ТВЕРДОЕ ТЕЛО – РАСТВОР При изучении адсорбции из растворов на твердых адсорбентах различают
- 74. Молекулярная адсорбция При молекулярной адсорбции из растворов (где участвуют 3 вещества) возможны 3 случая: положительная адсорбция
- 75. Молекулярная адсорбция Экспериментально величину адсорбции определяют зная начальную концентрацию раствора с0, объем раствора V и массу
- 76. Правило уравнивания полярностей (Ребиндера) Вещество С будет адсорбироваться на поверхности раздела фаз А и В если
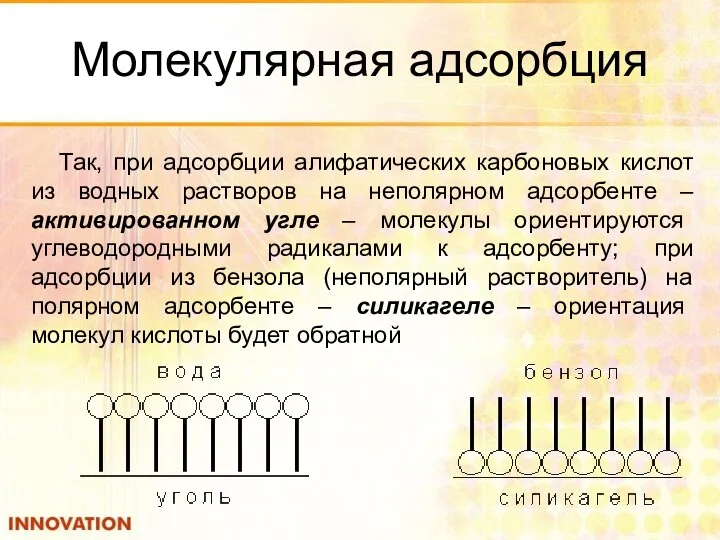
- 77. Молекулярная адсорбция Так, при адсорбции алифатических карбоновых кислот из водных растворов на неполярном адсорбенте – активированном
- 78. Вывод Из приведенного выше подтверждается тот факт, что: Для адсорбции ПАВ из неполярных или малополярных растворителей
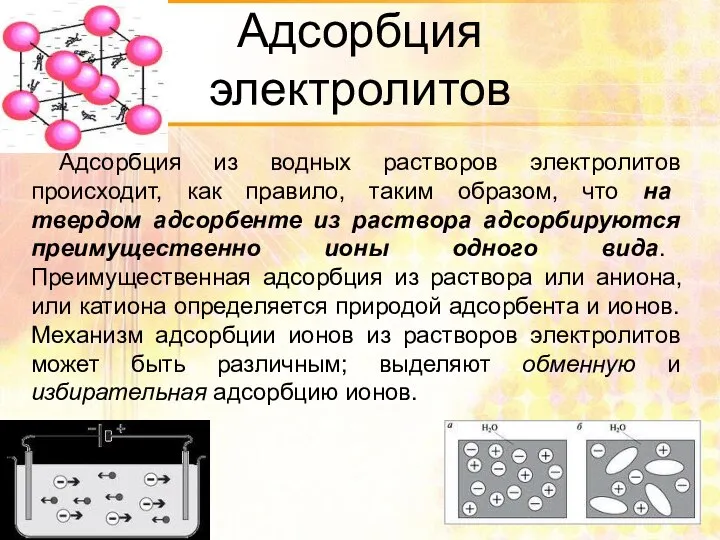
- 79. Адсорбция электролитов Адсорбция из водных растворов электролитов происходит, как правило, таким образом, что на твердом адсорбенте
- 80. Уравнение Никольского Процессы ионного обмена на твердой поверхности характеризуются уравнением Б.П.Никольского:
- 81. Обменная адсорбция представляет собой процесс обмена ионов между раствором и твердой фазой, при котором твердая фаза
- 82. Избирательная адсорбция Избирательная адсорбция не сопровождается выделением в раствор эквивалентного числа других ионов того же знака;
- 83. Правило Панета-Фаянса Из раствора адсорбируются те ионы, которые входят в состав кристаллической решетки сорбента или образуют
- 84. Ионообменная адсорбция Ионообменная адсорбция – процесс, в котором адсорбент и раствор обмениваются между собой в эквивалентных
- 85. Хроматография Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах сорбции и десорбции.
- 86. Хроматография – физико-химический метод, используется для разделения веществ аналитические цели препаративные цели Служит для идентификации и
- 87. Из истории хроматографии Михаил Семёнович Цвет (1872—1919) День рождения хроматографии – 21 марта 1903г. Доклад М.С.
- 88. капиллярная газовая хроматография (КГХ), высокоэффективная жидкостная хроматография (ВЭЖХ), высокоэффективная тонкослойная хроматография (ВЭТСХ), высокоэффективная ионная хроматография (ВЭИХ),
- 89. «Никакое другое открытие не оказало на исследования в органической химии такого огромного продолжительного влияния, как анализ
- 90. Принцип хроматографического разделения веществ Неподвижная фаза Подвижная фаза Молекулы разделяемых веществ Эффект разделения основывается на том,
- 91. Классификация методов хроматографии По типу агрегатного состояния фаз Газовая хроматография (ГХ) Жидкостная хроматография (ЖХ) летучие вещества,
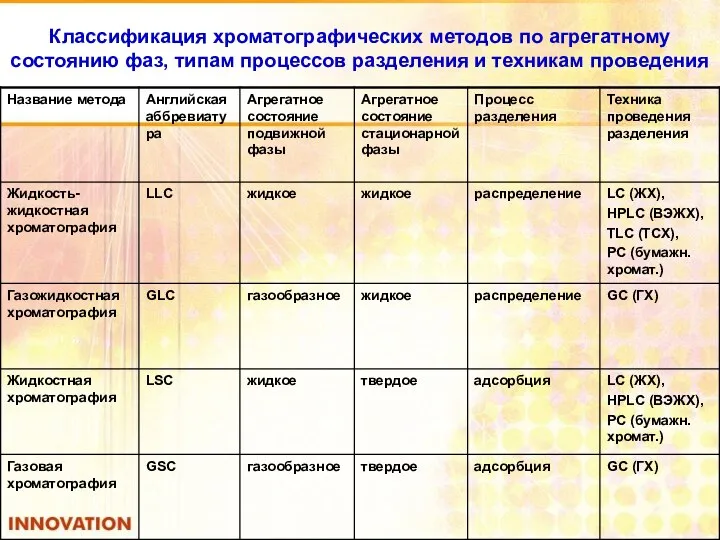
- 92. Классификация хроматографических методов по агрегатному состоянию фаз, типам процессов разделения и техникам проведения
- 93. Колоночная хроматография стационарная фаза находится в колонке; прием используется как в газовой, так и в жидкостной
- 94. Хроматограмма Хроматографический пик – концентрация пробы в подвижной фазе на выходе из колонки как функция времени.
- 95. Правильная запись данных ГЖХ Номер (шифр) эксперимента или номер образца Количество введенной пробы Используемая колонка (неподвижная
- 96. Газо-жидкостная хроматография (ГЖХ) Газо-жидкостная хроматография используется для разделения «летучих» соединений, т.е. соединений с молекулярной массой до
- 97. Аппаратурное оформление метода ГЖХ 1 – баллон с газом-носителем; 2 – стабилизатор потока; 3 и 3
- 98. Схема работы хроматографической колонки на примере капиллярной газовой хроматографии
- 99. Идентификация методом ГЖХ Для идентифицикации соединения в смеси, сравнивают его время удерживания с временем удерживания «подлинного»
- 100. Количественный анализ с использованием метода ГЖХ Wx = kxAx Wx – масса вещества, соответствующего пику с
- 101. Характеристики вещества, получаемые в хроматографическом методе Время удержания (время выхода) – время, проходящее между моментом ввода
- 102. ВЭЖХ Agilent Technologies
- 103. ВЭЖХ Милихром
- 104. ВЭЖХ HP
- 105. ВЭЖХ Люмекс
- 106. ВЭЖХ Чешский прибор
- 107. ГЖХ “Agilent Technologies”
- 108. ХМС НР
- 109. Энтеросорбция Метод лечения различных заболеваний, основанный на способности энтеросорбентов связывать и выводить из организма различные экзогенные
- 110. Энтеросорбенты ЭСБ – препараты медицинского назначения, обладающие высокой сорбционной емкостью, не разрушающиеся в ЖКТ и способные
- 111. Энтеросорбенты Полифепан (лигниг) Уголь активированный (сорбекс, карболонг, карболен)
- 112. Энтеросорбенты Смекта Кремнийорганический сорбент Энтеросгель
- 113. Энтеросорбция Энтеросорбция является составной частью эфферентной терапии (от латинского efferens — выводить), то есть группы лечебных
- 114. Гемодиализ Гемодиализ (от гемо- (от гемо- и др.-греч. (от гемо- и др.-греч. διάλυσις — разложение, отделение)
- 115. Перитонеальный диализ Перитонеальный диализ(анат. peritoneum брюшина: греч. dialysis разложение, отделение)метод очищения крови от эндогенных и экзогенных
- 116. Плазмаферез Мембранный плазмофильтр содержит камеры для протока крови, отделенные от камер сбора плазмы пористой мембраной. Мембрана
- 118. Скачать презентацию










































































































 Синтез лоратадина
Синтез лоратадина Белки. Теории строения белковой молекулы. (Тема 2)
Белки. Теории строения белковой молекулы. (Тема 2) Разбор контрольной работы. Химия (9 класс)
Разбор контрольной работы. Химия (9 класс) Теория химического строения органических соединений А.М. Бутлерова
Теория химического строения органических соединений А.М. Бутлерова Аминокислоты
Аминокислоты Свойства металлов и сплавов
Свойства металлов и сплавов Классификация неорганических веществ
Классификация неорганических веществ Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Углеводороды: изомерия
Углеводороды: изомерия Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) «Широко распростирает химия руки свои в дела человеческие! «Широко распростирает химия руки свои в дела человеческие! Куда ни
«Широко распростирает химия руки свои в дела человеческие! «Широко распростирает химия руки свои в дела человеческие! Куда ни Химические свойства металлов
Химические свойства металлов Спирты Предельные одноатомные спирты
Спирты Предельные одноатомные спирты Формы природных выделений минералов. Занятие 2
Формы природных выделений минералов. Занятие 2 Электрофизические и электрохимические методы обработки материалов
Электрофизические и электрохимические методы обработки материалов Спирттер және фенолдар
Спирттер және фенолдар Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач
Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач Токсическое действие сероводорода
Токсическое действие сероводорода Харчові добавки Підготували: Возна Руслана Таран Ірина
Харчові добавки Підготували: Возна Руслана Таран Ірина  Пищевые жиры
Пищевые жиры  Химия аминокислот, пептидов и белков
Химия аминокислот, пептидов и белков H2SiO3. Метакремниевая кислота
H2SiO3. Метакремниевая кислота Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат
Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Шампунь для волосся
Шампунь для волосся